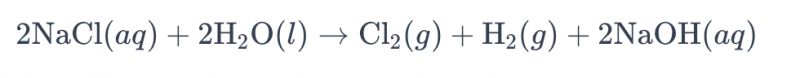Het proces waarbij een pekeloplossing wordt geëlektrolyseerd met behulp van titaniumelektroden om chloor te produceren, wordt gewoonlijk "elektrolyse van pekel" genoemd. Bij dit proces worden titaniumelektroden gebruikt om de oxidatiereactie van chloride-ionen in de pekel te bevorderen, wat leidt tot de vorming van chloorgas. De algemene chemische vergelijking voor de reactie is als volgt:
In deze vergelijking ondergaan chloride-ionen oxidatie aan de anode, wat resulteert in de productie van chloorgas, terwijl watermoleculen aan de kathode worden gereduceerd, waarbij waterstofgas ontstaat. Daarnaast ondergaan hydroxide-ionen reductie aan de anode, waarbij waterstofgas en natriumhydroxide worden gevormd.
De keuze voor titaniumelektroden is te danken aan de uitstekende corrosiebestendigheid en geleidbaarheid van titanium, waardoor de reactie tijdens de elektrolyse stabiel verloopt zonder te corroderen. Dit maakt titaniumelektroden een ideale keuze voor de elektrolyse van pekel.
Voor de elektrolyse van zout water is doorgaans een externe stroombron nodig om de energie voor de elektrolytische reactie te leveren. Deze stroombron is meestal een gelijkstroomvoeding (DC), omdat elektrolytische reacties een constante stroomrichting vereisen en een DC-voeding een constante stroomrichting kan leveren.
Bij het elektrolyseren van zout water om chloorgas te produceren, wordt doorgaans een laagspanningsgelijkstroomvoeding gebruikt. De spanning van de voeding is afhankelijk van de specifieke reactieomstandigheden en het ontwerp van de apparatuur, maar ligt over het algemeen tussen de 2 en 4 volt. Daarnaast is de stroomsterkte van de voeding een cruciale parameter die moet worden bepaald op basis van de grootte van de reactiekamer en de gewenste productieopbrengst.
Samenvattend hangt de keuze van de stroomvoorziening voor de elektrolyse van zout water af van de specifieke eisen van de experimenten of industriële processen, om een efficiënte reactie en het verkrijgen van de gewenste producten te garanderen.
Geplaatst op: 16 januari 2024